Оптимизация детоксикационной терапии у больных острыми кишечными инфекциями
19.08.19д.мед.н, проф. Малый В.П.1,
к.мед.н. Асоян І.М.1,Танчук Ю.В.2,
д.мед.н, проф. Нартов П.В.1,2,
к.мед.н. Маслова В.С.2
1 – Харьковская медицинская академия последипломного образования
2 – КНП ХОР «Обласная клиническая инфекционная больница»
Введение
Острые кишечные инфекции (ОКИ) представляют одну из наиболее актуальных проблем здравоохранения в мире (ВОЗ сообщает о ежегодной регистрации диарейных заболеваний в количестве более 1 млрд.), что наносит значительный социально-экономический ущерб [1, 2]. В настоящее время происходит изменение этиологических факторов ОКИ. Так, этиологическими факторами указанных инфекций чаще всего являются вирусы, хотя в Украине до настоящего времени не потеряли своей значимости бактериальные ОКИ (шигеллы, патогенные эшерихии, сальмонеллы, иерсинии и т.д.), а также условно-патогенная микрофлора (УПМ) [3, 4]. Заболевания имеют широкий диапазон клинических проявлений — от легких кишечных дисфункций вплоть до тяжелых форм с возможной генерализацией инфекции. От своевременности и адекватности назначения терапии при ОКИ зависят их и продолжительность заболевания и последствия (клинический исход) [5].
По современным представлениям, терапия указанных инфекций должна быть комплексной и этапной с индивидуальным подходом к выбору препаратов с расшифровкой этиологии, тяжести, фазы и клинической формы болезни и состояния макроорганизма к моменту заболевания [6]. Учитывая рост лекарственной резистентности возбудителей к широко применяемых антибактериальных препаратов, а также ограничения относительно их назначения, одним из методов этиопатогенетической терапии диареи является энтеросорбция [7]. Этиологическим фактором ОКИ в экономически развитых странах до 75-80% всех верифицированных случаев являются вирусные агенты (Koch J. et al., 2006; Kittigul L. et al., 2009; Bhattacharya SK et al., 2012), поэтому применение энтеросорбентов считают обоснованным благодаря способности фиксировать на своей поверхности бактерии и вирусы, которые находятся в полости кишечника и таким образом препятствовать генерализации инфекционного процесса не только бактериальной но и вирусной этиологии [15].
В многочисленных клинических исследованиях установлено, что при ОКИ, в патогенезе которых особое значение имеют адгезия, цитотоксическое действие возбудителей и ендотоксикоз, энтеросорбенты, в отличие от антибактериальных препаратов, оказывают быстрый и выраженный детоксикационный, гипотермический и антидиарейный клинический эффект. При этом за счет сорбции и элиминации из кишечника конкурентной патогенной и УНМ энтеросорбенты не оказывают негативного влияния на микробиоценоз кишечника [8]. Одним из существующих и зарегистрированных в Украине препаратов указанного действия является Энтероклин, который соответствует критериям «идеального» сорбента за счет наличия в своем составе высокодисперсного диоксида кремния, пектина, хитозана и лактулозы. Энтероклин обладает следующим спектром положительных эффектов [13, 14, 15]:
- имеет высокую эффективность благодаря большой площади активной поверхности и выводит из организма токсины, ионы тяжелых металлов;
- адсорбирует микроорганизмы и тормозит развитие болезнетворной микрофлоры благодаря диоксиду кремния в составе;
- способствует поддержанию нормальной микрофлоры кишечника;
- безопасный, без травматического воздействия на слизистую оболочку ЖКТ благодаря пектину в составе;
- отсутствует риск запора благодаря пектину и лактулозе;
- снижает кислотность желудочного сока, восстанавливает слизистую оболочку желудка благодаря хитозану в составе;
- препятствует потере витаминов и минералов;
- стимулирует неспецифический иммунитет;
- имеет нейтральный вкус, без вкусовых и ароматических добавок;
- имеет удобную форму выпуска и дозировку.
Целью работы было изучение эффективности энтеросорбента Энтероклин в комплексной терапии ОКИ.
Материалы и методы
Исследование выполнялось на клинической базе кафедры инфекционных болезней Харьковской медицинской академии последипломного образования КНП ХОР «Областная клиническая инфекционная больница».
Нами было обследовано 37 пациентов с ОКИ, из них 15 случайно отобранных получали терапию без назначения Энтероклина (группа сравнения), а 22 — дополнительно получали указанный энтеросорбент (основная группа) в дозе 1 пакет-саше 3 раза в сутки в течение 5 дней. Больные были обследованы в динамике — до и после лечения (рис. 1).
Дизайн исследования
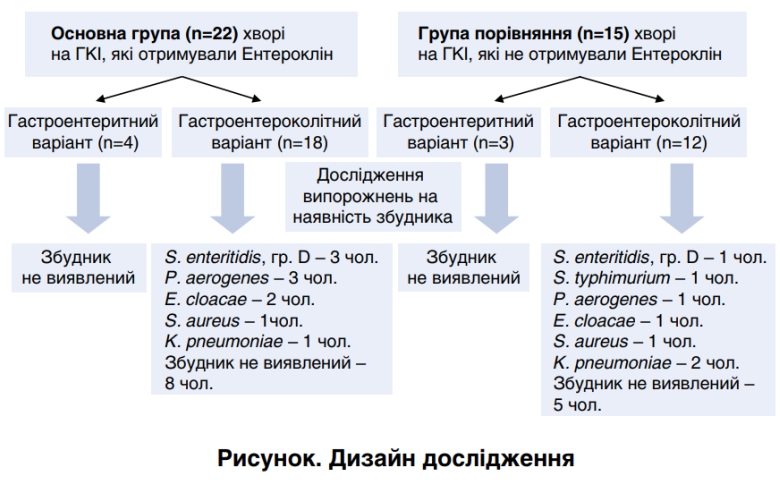
В основной группе больных гастроэнтеритный вариант ОКИ регистрировался в 18,2%, а гастроэнтероколитный — в 81,8%. В группе сравнения гастроэнтеритный вариант заболевания оказывался в 26,6%, а гастроэнтероколитный в 73,4%.
Среди основной группы больных мужчин было 9 (40,9%), а женщин 13 (59,1%). В группе сравнения лиц мужского пола было 6 (40%), а женщин 8 (60%). Средний возраст больных основной группы составил 34,6 лет, а группы сравнения — 36,7 лет.
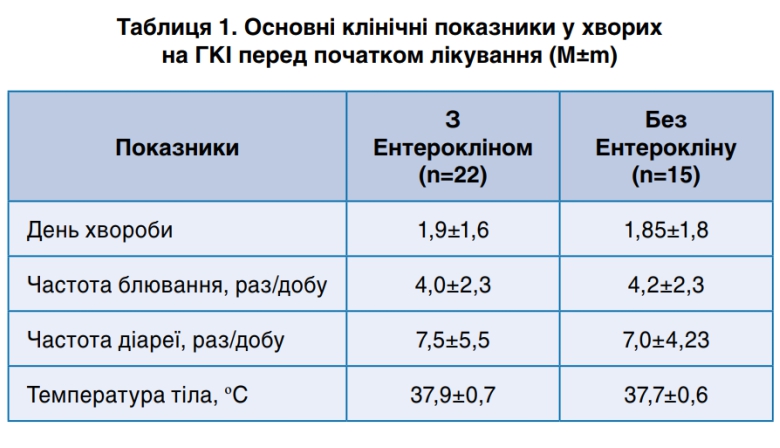
Данные, которые сгруппированы в табл. 1 свидетельствуют о том, что по основным клиническим показателям при поступлении в стационар больные в группах достоверно не отличались.
Клиническое обследование больных включало изучение жалоб, анамнеза жизни и заболевания, результатов объективного обследования, лабораторных данных (общий анализ крови и мочи), биохимические исследования крови в соответствии клинического состояния пациента и показаний, определения малонового диальдегида.
Статистическая обработка полученных результатов исследований осуществлялась с помощью программы STATISTIKA for Windows (StatSoftInc, США).
Результаты и обсуждение
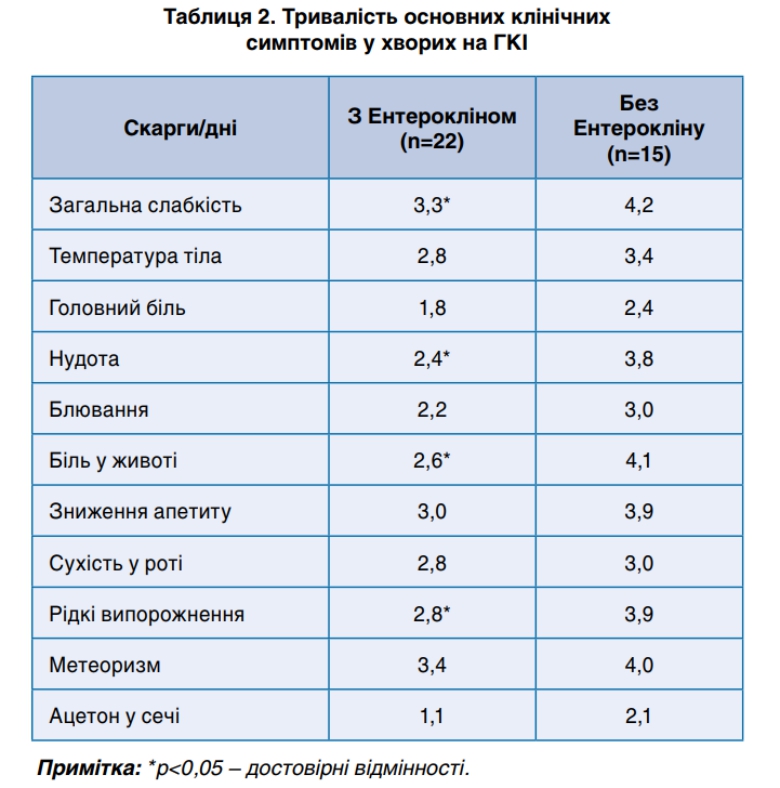
В нашем исследовании было обнаружено, что включение Энтероклина в стандартную терапию ОКИ существенно повлияло на течение заболевания, в частности привело к достоверному сокращению продолжительности основных клинических симптомов (табл. 2): общая слабость в среднем на 27,3% (р <0,05) , тошнота — на 58,3% (р <0,05), боль в животе — на 57,7% (р <0,05), жидкий стул — на 39,3% (р <0,05) по сравнению с пациентами, которым не назначался Энтероклин. В итоге симптомы интоксикации, локальных проявлений болезни, формирование нормального стула происходило статистически быстрее, чем у пациентов контрольной группы. И, как следствие, в основной группе больных наблюдалось статистически значимое (р <0,05) уменьшение на 30,0% (2,1 дня) продолжительности пребывания в стационаре по отношению к таким в группе сравнения.
Кроме того, у пациентов, которым назначался Энтероклин наблюдалось достоверное сокращение продолжительности кетонурии на 90,9% (р <0,05), чем у больных контрольной группы. Выявление ацетона в моче у больных ОКИ свидетельствует о наличии ацетонемического синдрома, ведь у таких пациентов последний является достаточно распространенным явлением связанным со рвотой и отсутствием приема пищи. В результате этого активируется липолиз, повышается в крови уровень свободных жирных кислот с последующим их метаболизмом в ацетилкоензим А в цикле трикарбоновых кислот Кребса, с синтезом кетоновых тел (ацетона, ацетоуксусной и β-оксимасляной кислот), снижается активность глюкозо-6-фосфатазы в печени.
Вместе с тем, на фоне инфекции возникает цитопатическое действие возбудителя на энтероцит с развитием вторичной лактазной недостаточности и диареи осмотического типа с накоплением большого количества летучих коротко цепных жирных кислот, водорода, углекислого газа и негидролизованних углеводов. Это приводит к активации потребления глюкозы с последующим снижением ее концентрации в крови, и способствует развитию метаболического ацидоза и ацетонемии. Образующиеся кетоновые тела окисляются в мышцах, миокарде, головном мозге до углекислого газа и воды, повышается уровень лактата и мочевой кислоты. Через развитие кетоацидоза наблюдается токсическое действие недоокисленных продуктов метаболизма на ЦНС приводит к вегетативным расстройствам, которые регистрировались у больных (потливость, тахикардия, тахипноэ, лихорадка), а иногда до рвоты, боли в животе спастического характера и т.д. [9, 10]. Поэтому назначение энтеросорбента Энтероклину привело к снижению эндогенной интоксикации, в том числе за счет кетоновых тел, что способствовало уменьшению их негативного воздействия на организм.
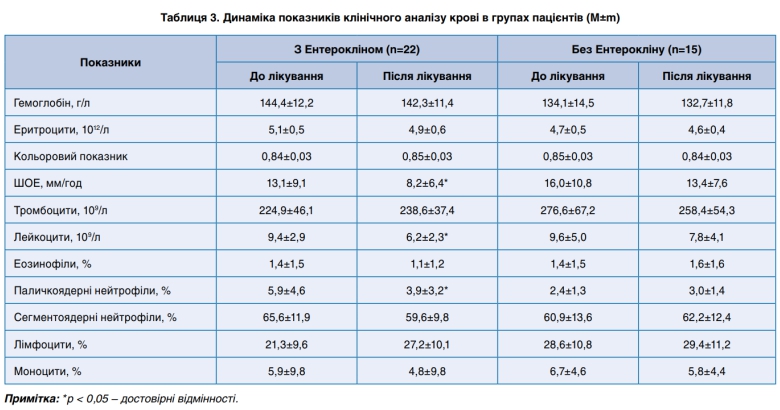
У пациентов, которым назначался Энтероклин, также наблюдалась более ранняя нормализация показателей клинического анализа крови (табл. 3), в частности СОЭ на 59,8% (р <0,05), количества лейкоцитов — на 51,6% (р <0, 05) и палочкоядерных нейтрофилив — на 51,3% (р <0,05) по сравнению с таковыми у больных, получавших терапию без Энтероклина, что свидетельствовало о более ранем угасании патологического процесса в организме.
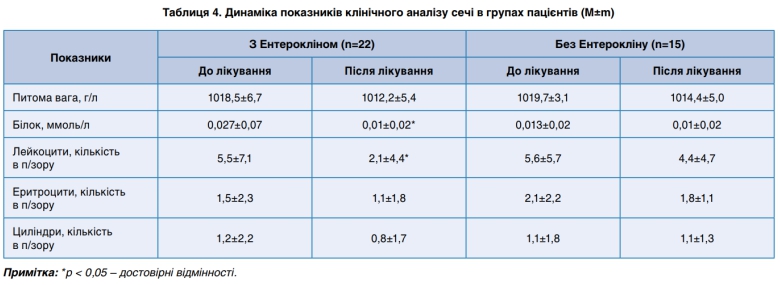
Терапия Энтероклином также способствовала существенному уменьшению содержания белка и лейкоцитов в клиническом анализе мочи (табл. 4). Включение препарата способствовало улучшению функции почек за счет сорбции токсинов и уменьшения их влияния на почечную ткань.
Важно отметить, что не угасает заинтересованность клиницистов в исследовании показателей перекисного окисления липидов (ПОЛ), как механизма, играющего большую роль в патогенезе ОКИ. Известно, что пусковым механизмом в развитии синдрома интоксикации являются бактериальные липополисахариды (ЛПС) — эндотоксины грамотрицательных микроорганизмов, а также продукты вторичного эндотоксикоза, образующиеся в организме в результате токсической агрессии извне и способны пролонгировать и усугублять интоксикацию.
Влияние ЛПС бактерий на активацию процессов ПОЛ активирует простагландиновый каскад, параллельно интенсифицирует свободно-радикальное окисление, продукты которого имеют прямое цитотоксическое действие, повреждают клеточные мембраны, тем самым вновь активизируют высвобождение субстрата для биосинтеза простагландинов. В связи с этим, изучение состояния антиоксидантной системы у больных ОКИ вызывает несомненный интерес в плане углубления представлений о патогенезе, показания к назначению патогенетической терапии, как критерий реконвалесценции. В качестве показателя активности прооксидантной системы наиболее известный малоновый диальдегид, который накапливается в крови и вызывает синдром интоксикации и используется для прогноза и контроля лечения [11, 12].
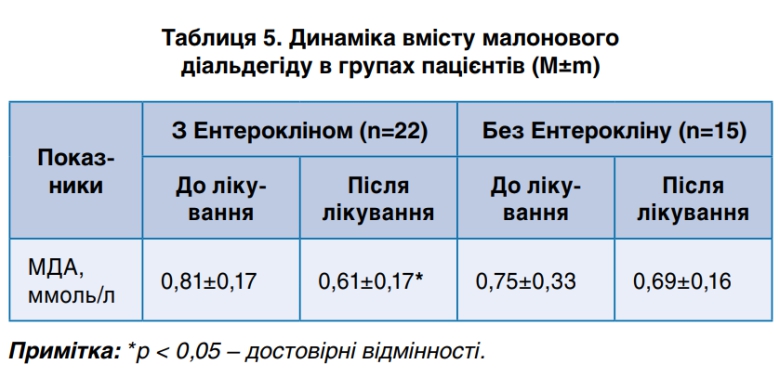
При назначении Энтероклина наблюдалось статистически значимое снижение уровня малонового диальдегида на 32,8% (р <0,05) по сравнению с таковыми в контрольной группе (табл. 5). Детоксикационная терапия Энтероклином привела к существенному снижению интенсивности ПОЛ, уменьшению оксидативного стресса в организме и купирования инфекционного процесса.
Выводы
- При выборе энтеросорбента для лечения ОКИ необходимо учитывать их сорбционную емкость, скорость поглощения токсичных соединений, селективность сорбции, а также наличие побочных явлений.
- Энтеросорбент Энтероклин является средством с многогранной эффективностью, определяемой детоксицирующим, антидиарейным и, возможно, этиотропным действием благодаря уникальному составу компонентов с сорбционной активностью. Включение препарата в комплексную терапию приводит к достоверному сокращению продолжительности общей слабости, тошноты, боли в животе, жидкого стула и кетонурии.
- Лечение Энтероклином ускорило нормализацию картины крови и мочи.
- Применение Энтероклина приводило к снижению уровня малонового диальдегида в динамике по сравнению с показателями контрольной группы, что свидетельствовало о снижении количества промежуточных продуктов ПОЛ, интенсивности оксидативного стресса и уменьшение эндогенной интоксикации в процессе лечения.
- Продолжительность пребывания больных в стационаре при применении энтеросорбента Энтероклин уменьшилось на 30,0% (р <0,05).
- Энтероклин может использоваться как важный высокоэффективный компонент терапии острых кишечных инфекций, как бактериальной, так и вирусной этиологии, независимо от тяжести болезни, а также от типа диареи.
Литература
- Acree M. Acute Diarrheal Infections in Adults / М. Acree, A. M. Davis // Jama. — 2017. — Т. 318. — №. 10. — С. 957-958.
- Riddle M. S. ACG clinical guideline: diagnosis, treatment, and prevention of acute diarrheal infections in adults / M. S. Riddle, H. L. DuPont, B. A. Connor // The American journal of gastroenterology. — 2016. — Т. 111. — №. 5. — С. 602.
- Малыш Н. Пути оптимизации эпидемиологического надзора за острыми кишечными инфекциями в Украине / Н.Г. Малыш, М.Д. Чемич, А.В. Кузьменко // Восточноукраинский медицинский журнал. — 2019. — Т. 7, № 1. — С. 28-38.
- Трихлеб В. И. Вспышки инфекционных заболеваний в странах мира, обусловленные употреблением пищевых продуктов / В. И. Трихлеб // Актуальная Инфектология. — 2018. — Т. 6, № 5. — С. 16-23.
- Инфекционным болезням: в 2 т. / Под ред. В. П. Малыша, М. А. Андрейчина. — Львов: «Магнолия», 2018. — Т. 1. — 652 с.
- Голубовская О. А. Современные подходы к диагностике и лечению диарейных заболеваний / А. А. Голубовская // Семейная медицина. — 2015. — №. 3. — С. 35-40.
- Бородин Ю. И. Биологические свойства сорбентов и перспективы их применения / Ю. И. Бородин, В. И. Коненков, В. Н. Пармон [и др.] // Успехи современной биологии. — 2014. — Т. 134. — № 3. — С. 236-248.
- Малый В.П. Острые кишечные инфекции с диарейным синдромом / В.П. Малый // Эпидемиология, гигиена, инфекционные болезни. — 2018. — № 1 (18). — С. 23-26.
- Анохин В. А. Ацетонемический синдром при острых кишечных инфекциях у детей / В. А. Анохин, С. В. Халиуллин, И. А. Гутор // Детские инфекции. — 2012. — Т. 11. — №. 1. — С. 6-12.
- Леженко Г. А. Место пробиотиков в терапии и профилактике возникновения вторичного ацетонемического синдрома / Г. А. Леженко, Е. Е. Пашкова // Здоровье ребенка. — 2015. — №. 3 (63). — С. 31-34.
- Одинец Т.Н. Состояние антиэндотоксинового иммунитета и метаболической интоксикации при острых кишечных инфекциях / Т.Н. Одинец, И.З. Каримов, Д.К. Шмойлов [и др.] // Актуальная Инфектология — 2014. — №2 (3). — С. 27-29.
- Маржохова М. Ю. Некоторые показатели синдрома интоксикации при острых кишечных инфекциях / М. Ю. Маржохова, М. А. Башиева, Ж. М. Желихажева // Эпидемиология и инфекционные болезни. — 2008. — № 6. — С. 39-42.
- Лурин И.А., Сотников А.В., «Микробный пейзаж и чувствительность к антибиотикам возбудителей анаэробных неклостридиальные флегмоны таза» // Таврический МЕДИКО-БИОЛОГИЧЕСКИЙ ВЕСТНИК 2011, том 14, №4 ч.1 (56)
- Инструкция к применению препарата ЭНТЕРОКЛИН®, ТУ У 10.8-38405950-005: 2016.
- Крамарев С.А., Дмитриева О.А., Национальный медицинский университет имени А.А. Богомольца, г.. Киев, «ЭНТЕРОСОРБЦИЯ при острых кишечных инфекциях у детей» // ЖУРНАЛ «ЗДОРОВЬЕ РЕБЕНКА» 2 (29) 2011
Журнал «Клінічна імунологія. Алергологія. Інфектологія» № 5 (118) ‘2019, стр. 42-45
